Fivevet chia sẻ đầy đủ quy trình bảo quản đông lạnh tế bào dòng: chuẩn bị tế bào, chọn môi trường trữ đông, kiểm soát nhiệt độ và đánh giá chất lượng sau rã đông, giúp tối ưu hiệu quả nghiên cứu.

Quy trình bảo quản đông lạnh tế bào dòng
I. Vì sao bảo quản đông lạnh tế bào dòng là tiêu chuẩn vàng trong nghiên cứu hiện đại?
Trong nghiên cứu y sinh và công nghệ sinh học hiện đại, việc bảo tồn nguồn tế bào ổn định và lâu dài đóng vai trò vô cùng quan trọng. Từ các dòng tế bào nghiên cứu cơ bản, tế bào gốc, tế bào miễn dịch cho đến các chủng vi sinh vật phục vụ sản xuất vắc xin và dược phẩm, tất cả đều cần được lưu trữ theo phương pháp đảm bảo duy trì đặc tính sinh học ban đầu. Trong đó, kỹ thuật bảo quản đông lạnh sâu bằng nitơ lỏng ở nhiệt độ -196°C được xem là tiêu chuẩn vàng nhờ khả năng ngừng gần như hoàn toàn các hoạt động chuyển hóa của tế bào.
Tuy nhiên, quá trình cất giống không chỉ đơn giản là làm lạnh tế bào mà đòi hỏi kiểm soát chặt chẽ từ khâu chuẩn bị, sử dụng chất bảo vệ đông đến tốc độ hạ nhiệt và điều kiện lưu trữ. Nếu thực hiện không đúng, tế bào có thể giảm khả năng sống hoặc thay đổi đặc tính sau rã đông. Vì vậy, việc nắm rõ các lưu ý quan trọng trong quá trình đông lạnh và bảo quản là yếu tố quyết định đến chất lượng mẫu tế bào lưu trữ.
II. Nguyên lý của bảo quản đông lạnh chậm tế bào
2.1. Ảnh hưởng của nhiệt độ thấp lên tế bào
Khi tế bào được làm lạnh đến rất thấp (như trong nitơ lỏng −196°C), hầu hết các hoạt động sinh học bị ngừng lại, giúp mẫu giữ được đặc tính gần như ban đầu trong thời gian dài. Tuy nhiên, nguy cơ tổn thương lớn nhất không phải do nhiệt độ thấp trực tiếp, mà là do hình thành tinh thể băng trong và ngoài tế bào, gây sốc thẩm thấu và tổn thương màng tế bào khi nước đóng băng trong khoảng nhiệt độ chuyển tiếp (~0 đến −40°C).
2.2. Cơ chế hình thành tinh thể băng nội bào và ngoại bào
Trong quá trình đông lạnh, nước ở môi trường bên ngoài tế bào sẽ đóng băng trước, tạo thành các tinh thể băng ngoại bào. Khi đó, nồng độ chất hòa tan bên ngoài tăng cao, kéo nước từ trong tế bào ra ngoài theo cơ chế thẩm thấu, khiến tế bào dần bị mất nước.
Nếu tốc độ làm lạnh quá nhanh, nước bên trong tế bào không kịp thoát ra ngoài mà sẽ đóng băng ngay trong tế bào, hình thành tinh thể băng nội bào. Đây là nguyên nhân gây tổn thương cơ học nghiêm trọng, làm giảm tỷ lệ sống của tế bào sau khi rã đông.
2.3. Vai trò của chất bảo vệ đông (Cryoprotectant – CPA)
Để hạn chế tổn thương do tinh thể băng trong quá trình đông lạnh, người ta sử dụng chất bảo vệ đông (cryoprotectants – CPA). Các CPA có vai trò:
- Giảm nhiệt độ đóng băng, kéo dài khoảng siêu lạnh không tạo tinh thể.
- Tăng độ nhớt của dịch tế bào, hạn chế sự hình thành tinh thể.
- Ổn định màng tế bào và làm giảm sốc thẩm thấu.
Cryoprotectants (CPA) được chia thành hai nhóm:
- Có thể thấm qua màng tế bào (như DMSO, glycerol).
- Không thấm (như sugars), tùy mục đích sử dụng.
DMSO là CPA thấm qua màng tế bào phổ biến nhất trong nhiều quy trình bảo quản tế bào động vật. Nó giúp làm giảm hình thành tinh thể băng bằng cách làm tăng nồng độ solute nội bào và giảm nhiệt độ đóng băng của nước, từ đó tăng khả năng sống sót của tế bào sau rã đông. Tuy nhiên, DMSO cũng có độc tính nhất định nên phải sử dụng ở nồng độ tối ưu và loại bỏ nhanh sau khi rã đông.
Glycerol cũng là CPA thấm qua màng và được dùng rộng rãi trong bảo quản tinh trùng và một số tế bào, đặc biệt trong các ứng dụng liên quan đến mô hoặc dịch sinh học. Glycerol làm tăng osmolarity của môi trường và hạn chế sự hình thành băng, tương tự DMSO, nhưng thấm vào tế bào chậm hơn nên thường cần thời gian cân bằng dài hơn trước khi đóng băng.
Phương pháp đông lạnh chậm có kiểm soát giúp kiểm soát tốc độ làm lạnh ở mức chậm và ổn định (thường khoảng −1°C/phút). Mục tiêu là cho nước thoát ra dần khỏi tế bào trước khi kết tinh, hạn chế tinh thể nội bào và giảm tổn thương. CPA được dùng ở nồng độ vừa phải, dễ thao tác trong phòng thí nghiệm. Đây là cách phổ biến nhất trong bảo quản tế bào nuôi cấy và mô rời.
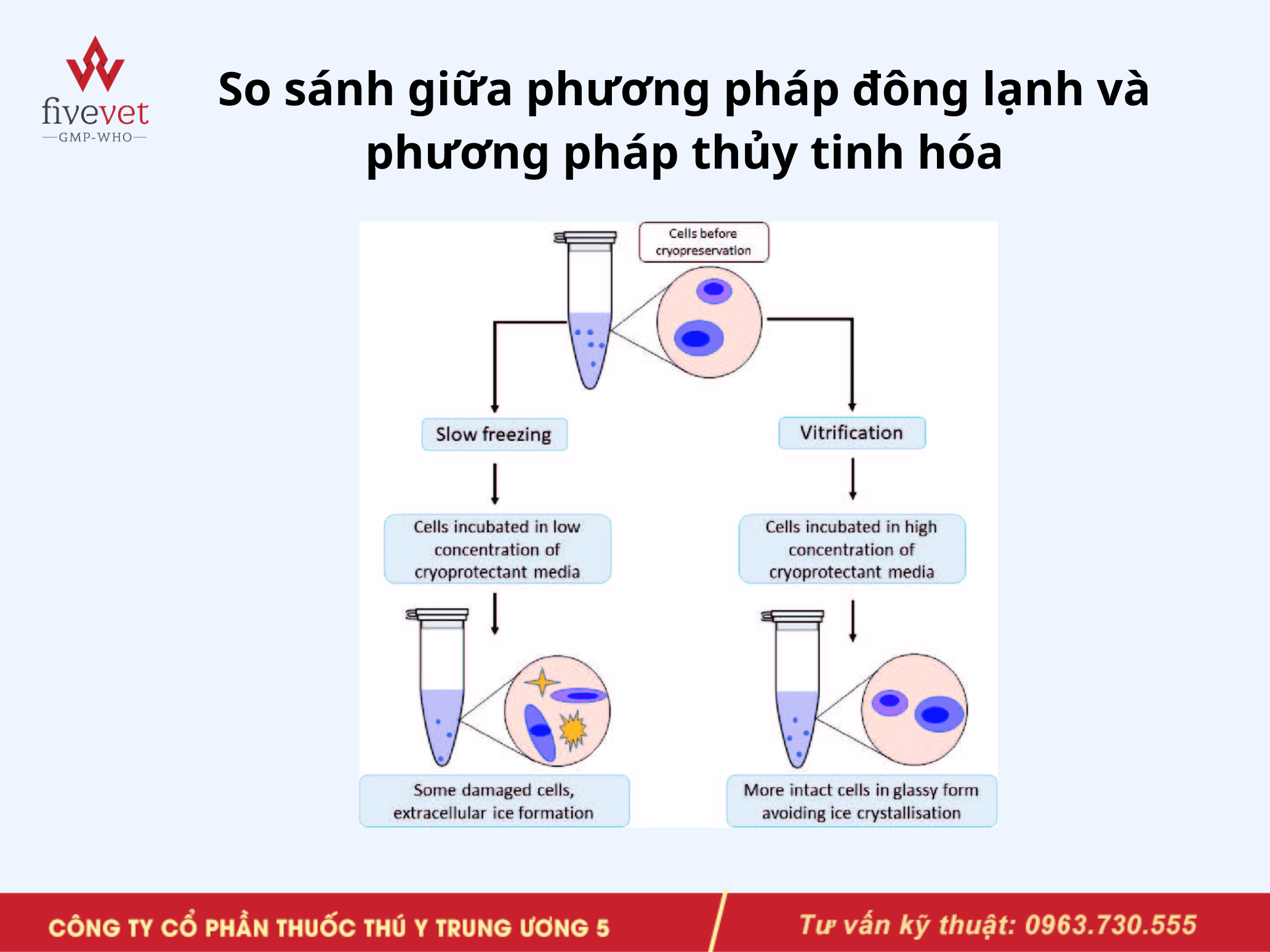
So sánh giữa phương pháp đông lạnh và phương pháp thủy tinh hóa
III. Quy trình bảo quản đông lạnh tế bào dòng
3.1. Chuẩn bị trước khi cất giống
Chất lượng tế bào trước khi trữ đông quyết định trực tiếp tỷ lệ sống sau rã đông. Tế bào nên được thu ở pha tăng trưởng log (logarithmic phase), là giai đoạn đang nhân lên tích cực, vì trong giai đoạn này tế bào khỏe mạnh và ít bị stress hơn, giúp tỷ lệ sống sau rã đông cao hơn. Việc đông lạnh tế bào ở giai đoạn vượt quá confluency hoặc suy yếu sẽ làm giảm khả năng phục hồi sau đó. Đồng thời, phải đảm bảo độ sống cao (thường >90%) trước khi đóng băng để tối ưu hóa kết quả thu được sau rã đông. Tế bào cần được kiểm tra vô trùng, không tạp nhiễm vi khuẩn, nấm và đặc biệt là Mycoplasma để không ảnh hưởng đến nghiên cứu sau này.
Mật độ tế bào khi trữ đông
Mật độ tế bào khi trữ đông cũng rất quan trọng. Nếu quá thấp, tế bào dễ bị stress; quá cao, lại làm giảm hiệu quả trao đổi và ảnh hưởng đến sự phân bố CPA, dẫn đến tỷ lệ sống sau rã đông kém hơn. Mật độ tối ưu thường được khuyến cáo từ khoảng 1x10⁶ đến 5x10⁶ tế bào/ml, tùy loại mẫu.
Thành phần môi trường đông lạnh
Môi trường trữ đông thường gồm:
- Môi trường nuôi cấy cơ bản (như DMEM, MEM,…)
- Huyết thanh (FBS)
- Chất bảo vệ đông (CPA) như DMSO
DMSO là CPA thấm qua màng tế bào phổ biến nhất, có khả năng giảm hình thành tinh thể băng và bảo vệ màng tế bào khi hạ nhiệt. Các nghiên cứu chỉ ra nồng độ DMSO thường dùng khoảng 5–10% là phù hợp với nhiều loại tế bào để đạt tỷ lệ sống sau rã đông cao nhất mà không vượt quá mức độc tính của DMSO.
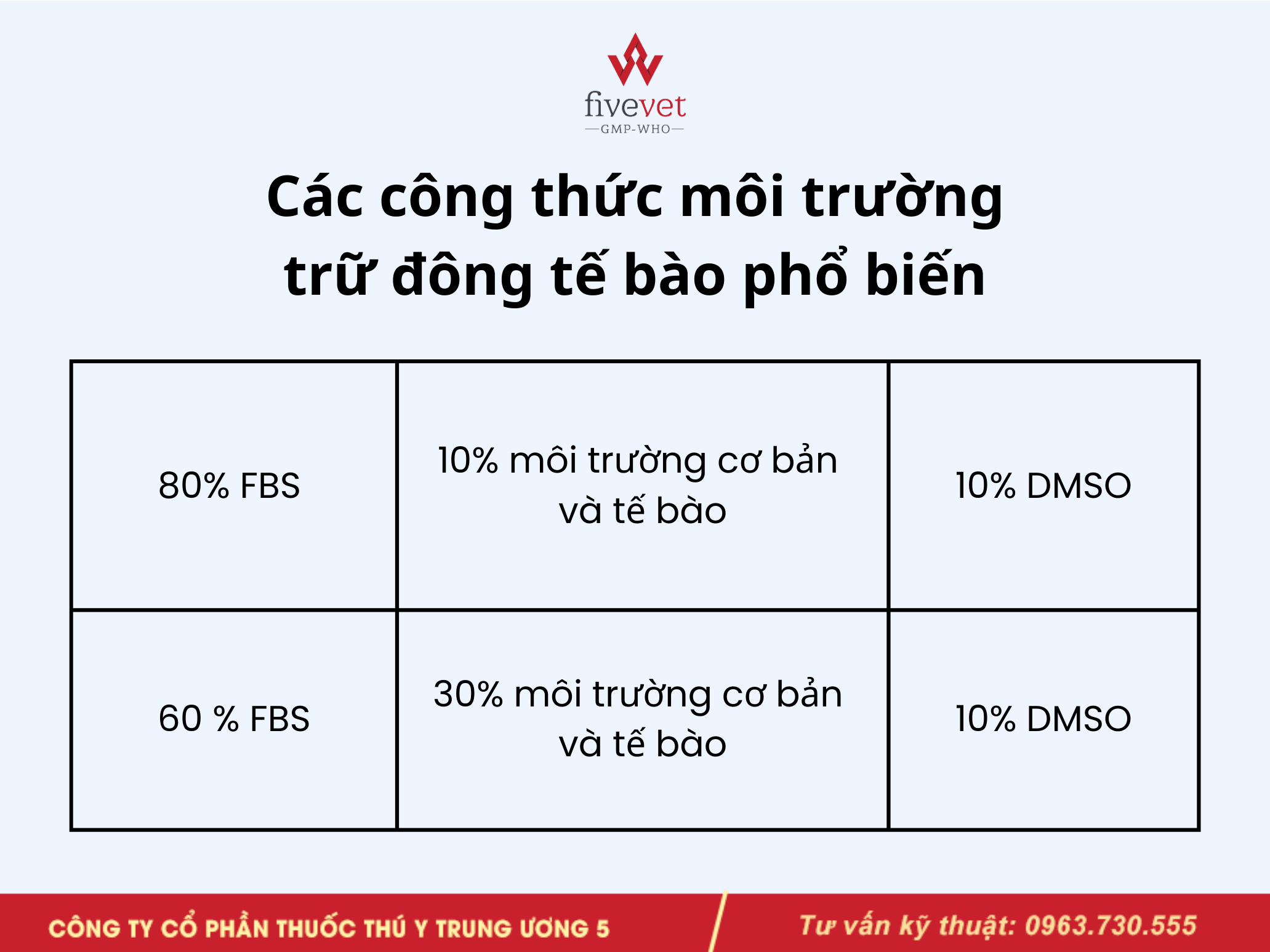
Các công thức môi trường trữ đông tế bào phổ biến
Lưu ý:
- Pha môi trường đông trên đá lạnh
- Lọc môi trường qua lọc vô trùng (0.22 µm)
- Giữ lạnh trước khi sử dụng để giảm độc tính DMSO
Sử dụng ống cryovial chất lượng cao chịu lạnh sâu, có nắp kín để tránh rò rỉ và nhiễm chéo. Nên dùng loại phù hợp với hệ thống lưu trữ nitơ lỏng và kiểm soát nhiệt độ. Trên mỗi ống phải ghi rõ thông tin tối thiểu: tên dòng tế bào, passage, mật độ tế bào, ngày đông, CPA sử dụng và người thực hiện.
Ghi nhãn rõ ràng giúp quản lý mẫu lâu dài và tránh nhầm lẫn trong kho lưu trữ. Biểu mẫu theo dõi: Thiết kế bảng theo dõi quy trình và điều kiện lưu trữ (như mức nitơ lỏng, vị trí ống, ngày kiểm tra) là yếu tố cần thiết trong quản lý chất lượng phòng thí nghiệm. Việc này hỗ trợ truy vết và đảm bảo thực hành chuẩn trong các kho lưu trữ tế bào.
3.2. Quy trình trữ đông tế bào
a. Thu hoạch tế bào
Với tế bào bám dính:
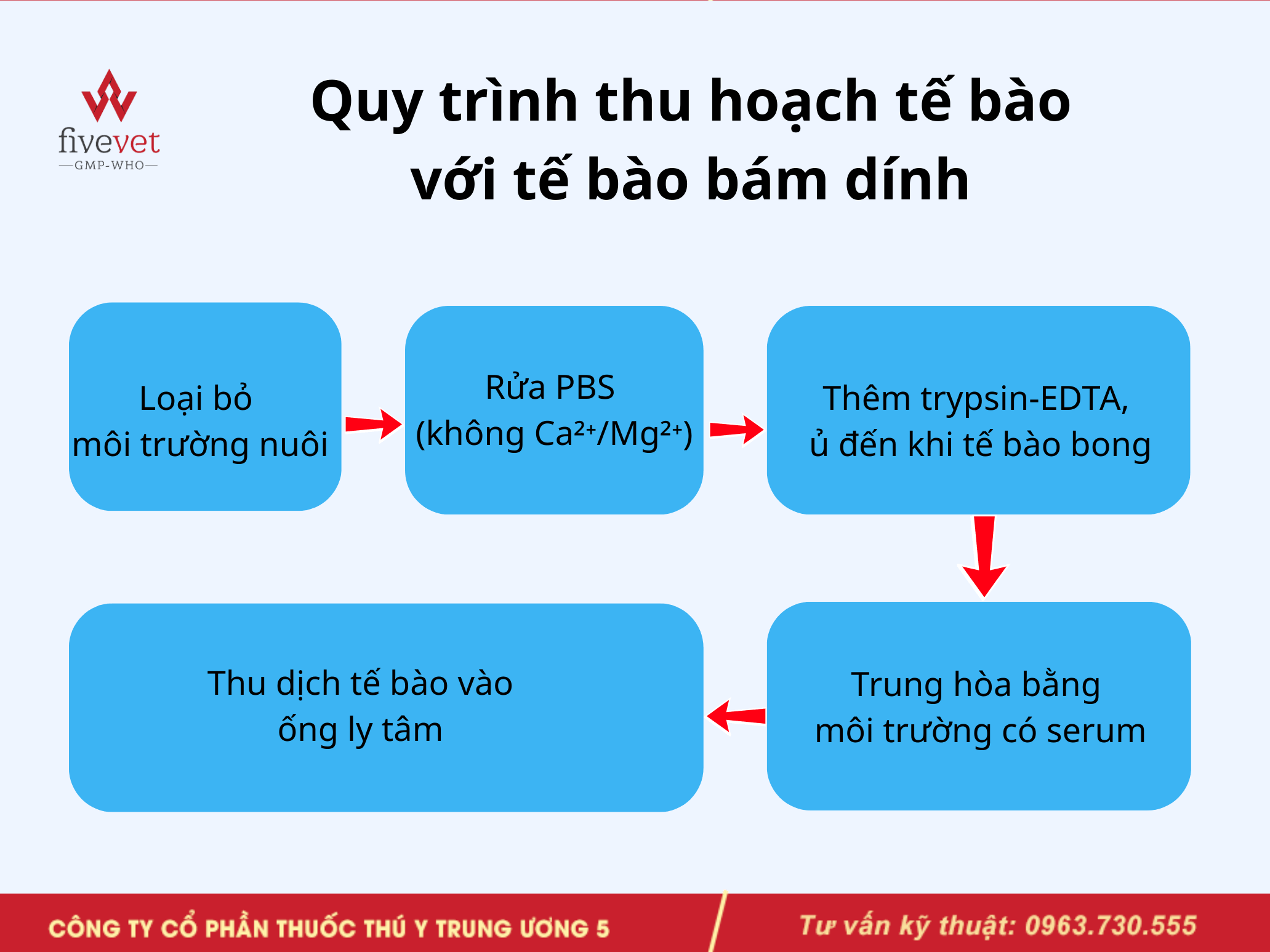
Quy trình thu hoạch tế bào với tế bào bám dính
Với tế bào huyền phù:
Thu trực tiếp dịch nuôi vào ống ly tâm. Thực hiện ly tâm 300-400 vòng trong 5 phút và loại bỏ dịch nổi.
b. Pha tế bào với môi trường đông
- Hoàn nguyên tế bào và xác định tỷ lệ sống/chết bằng Trypan Blue 0,4%.
- Điều chỉnh mật độ tế bào, thông thường 1–5 × 10⁶ tế bào/ml.
- Trộn tế bào với môi trường đông lạnh chứa DMSO nhẹ nhàng, tránh tạo bọt.
- Chia tế bào vào mỗi cryovial, thao tác nhanh nhưng nhẹ nhàng để giảm thời gian tiếp xúc DMSO ở nhiệt độ phòng.
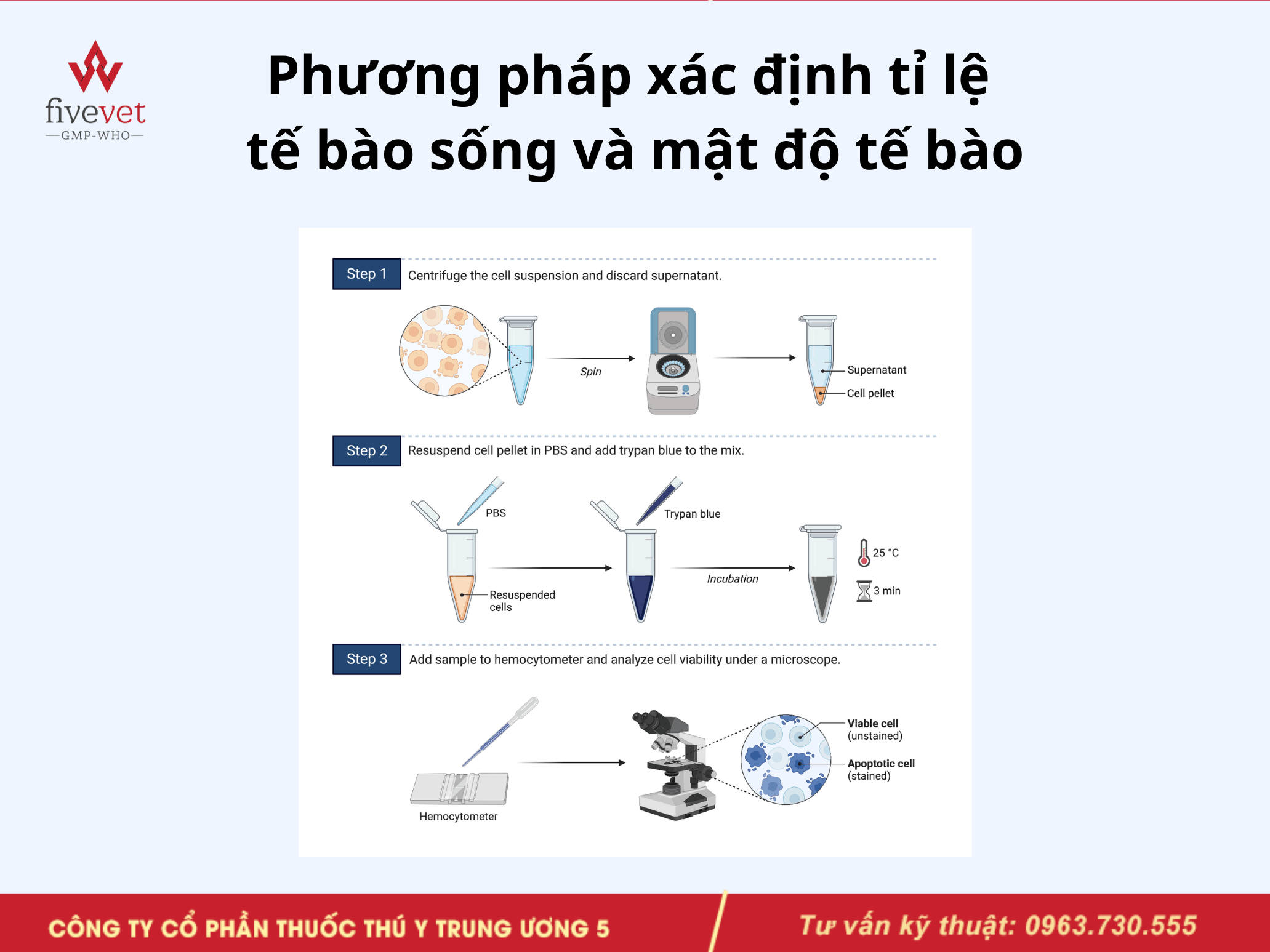
Phương pháp xác định tỉ lệ tế bào sống và mật độ tế bào
Làm lạnh có kiểm soát:
Sau khi tế bào đã được chia vào cryovial với môi trường đông chứa DMSO:
- Đặt các cryovial vào hộp làm lạnh chuyên dụng để đảm bảo tốc độ hạ nhiệt khoảng -1°C/phút
- Chuyển vào tủ −80°C và giữ trong 12–24 giờ
Tốc độ làm lạnh chậm giúp nước thoát dần khỏi tế bào, giảm hình thành tinh thể băng nội bào và tăng tỷ lệ sống sau rã đông.
Bảo quản:
Sau giai đoạn ổn định ở -80°C, các cryovial được chuyển nhanh sang bình nitơ lỏng (-196°C) để bảo quản lâu dài. Ở nhiệt độ này, hầu hết hoạt động sinh học bị ngừng hoàn toàn, giúp duy trì tính ổn định của tế bào trong nhiều năm.
Mẫu có thể được bảo quản trong:
- Pha lỏng (ngập trực tiếp trong nitơ)
- Pha hơi (phía trên bề mặt nitơ lỏng)
3.3 Rã đông và đánh giá chất lượng tế bào sau bảo quản
Sau khi tế bào đã được bảo quản trong nitơ lỏng, việc rã đông nhanh và an toàn là điều kiện quan trọng để tối đa hóa khả năng sống sót và đảm bảo tế bào phục hồi chức năng bình thường.
Các nghiên cứu cho thấy việc rã đông nhanh giúp giảm thời gian tế bào tiếp xúc với các tinh thể băng đang tan và hạn chế tổn thương do chuyển pha, đặc biệt khi nước chuyển từ rắn sang lỏng có thể tái kết tinh gây tổn hại màng tế bào nếu làm chậm.
Rã đông nhanh, đúng kỹ thuật:
Phương pháp chuẩn là sử dụng bồn nước 37°C, đưa cryovial vào bồn nước ấm đến khi chỉ còn rất ít băng trong ống, thường chỉ mất vài giây đến 1 phút, để đạt rã đông nhanh nhất mà vẫn an toàn cho tế bào. Nhiều hướng dẫn hiện nay vẫn khuyến cáo tốc độ rã đông nhanh ở khoảng 37°C vì đây là điều kiện gia nhiệt hiệu quả, giúp phục hồi tốt hơn các tế bào sau bảo quản lạnh sâu.
Loại bỏ CPA sau rã đông:
Ngay sau khi rã đông, CPA như DMSO cần được loại bỏ càng sớm càng tốt vì tính nhạy cảm và độc tính của nó đối với tế bào ở nhiệt độ sinh học.
Quy trình thường gồm pha loãng dần bằng cách thêm môi trường nuôi cấy ấm giàu huyết thanh và chất dinh dưỡng vào ống chứa tế bào rã đông để giảm nồng độ DMSO, sau đó ly tâm nhẹ để tách tế bào khỏi dịch chứa CPA và loại bỏ phần dịch chứa DMSO. Việc pha loãng và ly tâm giúp giảm sốc thẩm thấu và độc tính CPA, hỗ trợ tế bào trở lại trạng thái sinh trưởng bình thường.
Đánh giá chất lượng tế bào sau rã đông:
Sau bảo quản lạnh, cần kiểm tra các chỉ số quan trọng:
- Tỷ lệ sống (viability): đánh giá ngay sau rã đông và sau thời gian phục hồi trong môi trường nuôi cấy.
- Hình thái tế bào: tế bào bình thường sẽ phục hồi hình thái đặc trưng khi quan sát dưới kính hiển vi trong vài giờ đến vài ngày sau rã đông.
- Khả năng tăng sinh: tế bào nên được nuôi cấy tiếp sau rã đông để kiểm tra khả năng tăng trưởng và nhân lên; các tế bào khỏe mạnh sẽ duy trì tỷ lệ phân chia tương tự khi chưa trải qua bảo quản lạnh sâu.
3.4. Các rủi ro thường gặp khi trữ đông tế bào và biện pháp phòng ngừa
a. Tế bào chết nhiều sau rã đông
Đây là vấn đề phổ biến nhất khi trữ đông tế bào. Nguyên nhân thường do:
- Tế bào ban đầu kém chất lượng (không ở pha log, độ sống thấp).
- Nồng độ hoặc thời gian tiếp xúc DMSO không phù hợp.
- Tốc độ làm lạnh không đạt chuẩn (quá nhanh hoặc quá chậm).
- Rã đông chậm làm tăng tái kết tinh băng.
Biện pháp phòng ngừa:
- Chỉ trữ đông tế bào khỏe, độ sống ≥ 90%.
- Sử dụng nồng độ DMSO tối ưu (thường 5–10%) và hạn chế thời gian tiếp xúc ở nhiệt độ phòng. Lọc DMSO cũng như môi trường trữ đông qua lọc vô trùng 0,22µm.
- Đảm bảo tốc độ hạ nhiệt khoảng -1°C/phút.
- Rã đông nhanh ở 37°C và loại bỏ DMSO sớm.
- Thực hiện thử nghiệm tối ưu hóa quy trình cho từng loại tế bào.
b. Nhiễm chéo giữa các mẫu
Nhiễm chéo có thể xảy ra do ống không kín, nitơ lỏng bị nhiễm vi sinh vật, hoặc thao tác không đảm bảo vô trùng. Nếu một mẫu bị nhiễm, nguy cơ lan sang mẫu khác trong cùng bình là có thể xảy ra, đặc biệt khi bảo quản ở pha lỏng.
Biện pháp phòng ngừa:
- Đảm bảo ống cryovial kín và đạt tiêu chuẩn lưu trữ lạnh sâu.
- Ưu tiên bảo quản ở pha hơi nitơ để giảm nguy cơ tiếp xúc trực tiếp với nitơ lỏng.
- Không lưu trữ mẫu nghi nhiễm chung với mẫu sạch.
- Kiểm tra định kỳ tình trạng nhiễm Mycoplasma và vi sinh vật.
c. Tai nạn do nitơ lỏng
Nitơ lỏng có nhiệt độ cực thấp (-196°C) và có thể gây bỏng lạnh nghiêm trọng khi tiếp xúc trực tiếp với da hoặc mắt. Ngoài ra, sự bay hơi của nitơ có thể làm giảm nồng độ oxy trong phòng kín, gây nguy cơ ngạt. Ống cryovial nếu không kín hoàn toàn có thể phát nổ khi rã đông do nitơ thâm nhập vào bên trong.
Biện pháp phòng ngừa:
- Trang bị đầy đủ bảo hộ cá nhân: găng tay chống lạnh, kính bảo hộ, áo choàng.
- Làm việc trong khu vực thông thoáng, tránh không gian kín.
- Không đậy kín hoàn toàn nắp bình khi có nguy cơ tích tụ áp suất.
- Kiểm tra định kỳ tình trạng bình chứa và mức nitơ.
- Tuân thủ quy trình an toàn sinh học và an toàn hóa chất của phòng thí nghiệm.
IV.Các yếu tố quyết định hiệu quả trữ đông tế bào dòng
Bảo quản đông lạnh tế bào trong nitơ lỏng là kỹ thuật nền tảng trong nghiên cứu và ứng dụng sinh học hiện đại. Hiệu quả trữ đông phụ thuộc vào nhiều yếu tố quan trọng:
- Chất lượng tế bào trước khi đông (đúng pha tăng trưởng, độ sống cao, không nhiễm vi sinh)
- Lựa chọn và sử dụng chất bảo vệ đông với nồng độ tối ưu
- Kiểm soát tốc độ làm lạnh khoảng −1°C/phút
- Lưu trữ ở nhiệt độ dưới −130°C
- Rã đông nhanh và loại bỏ CPA đúng cách
Chỉ cần sai lệch ở một bước cũng có thể làm giảm tỷ lệ sống, ảnh hưởng đến hình thái và chức năng sinh học của tế bào sau bảo quản.
Bên cạnh yếu tố kỹ thuật, việc chuẩn hóa quy trình (SOP) và quản lý chất lượng hệ thống lưu trữ đóng vai trò quyết định trong duy trì tính ổn định và độ tin cậy lâu dài của mẫu. Ghi nhãn đầy đủ, quản lý vị trí mẫu rõ ràng, theo dõi mức nitơ định kỳ và kiểm soát nhiễm chéo không chỉ giúp bảo vệ nguồn mẫu quý giá mà còn đảm bảo tính chính xác và khả năng truy xuất trong nghiên cứu.
Do đó, trữ đông tế bào không chỉ là một thao tác kỹ thuật mà là một quy trình tổng thể đòi hỏi sự tuân thủ nghiêm ngặt, đào tạo bài bản và kiểm soát chất lượng liên tục để đạt hiệu quả tối ưu.
Bài viết được biên soạn bởi Phòng Nghiên cứu phát triển Vắc xin- Công ty cổ phần thuốc thú y Trung ương 5 (Fivevet).
Câu hỏi thường gặp:
1. Vì sao phải trữ đông tế bào trong nitơ lỏng?
Nitơ lỏng (−196°C) giúp ngừng hầu hết hoạt động sinh học của tế bào, từ đó bảo quản ổn định đặc tính ban đầu trong thời gian dài mà không làm biến đổi cấu trúc hay chức năng.
2. Vì sao phải kiểm soát tốc độ làm lạnh khoảng −1°C/phút?
Tốc độ làm lạnh chậm, ổn định giúp nước thoát dần khỏi tế bào trước khi kết tinh, hạn chế hình thành tinh thể băng nội bào và tăng tỷ lệ sống sau rã đông.
3. Tại sao cần rã đông nhanh ở 37°C?
Rã đông nhanh giúp giảm tái kết tinh tinh thể băng khi chuyển pha từ rắn sang lỏng, từ đó hạn chế tổn thương màng tế bào và cải thiện khả năng phục hồi.
4. Các chỉ số quan trọng để đánh giá tế bào sau rã đông có đạt chất lượng là gì?
Cần kiểm tra:
- Tỷ lệ sống (viability)
- Hình thái tế bào dưới kính hiển vi
- Khả năng tăng sinh sau vài ngày nuôi cấy
5. Vì sao cần xây dựng SOP trong trữ đông tế bào?
Quy trình chuẩn (SOP) giúp đồng bộ thao tác, kiểm soát chất lượng, giảm sai sót và đảm bảo khả năng truy xuất mẫu trong nghiên cứu dài hạn.
Xem thêm:
Tài liệu tham khảo:
- Cryopreservation: An Overview of Principles and Cell-Specific Considerations - PMC
- Principles of cryopreservation - PubMed
- Overcoming ice: cutting-edge materials and advanced strategies for effective cryopreservation of biosample | Journal of Nanobiotechnology | Springer Nature Link
- Principles of cryopreservation - PubMed
- Cryopreservation: An Overview of Principles and Cell-Specific Considerations - PMC
- The Impact of Varying Cooling and Thawing Rates on the Quality of Cryopreserved Human Peripheral Blood T Cells | Scientific Reports
- Rủi ro của Protein và DMSO trong Bảo quản đông lạnh: Thách thức trong việc Bảo quản các tế bào nhạy cảm cho Liệu pháp tế bào và gen - Atlantis Bioscience Pte Ltd
- The impact of cryopreservation on bone marrow-derived mesenchymal stem cells: a systematic review - PMC